Confira questões resolvidas sobre o Equilíbrio Químico:
1) UFRGS – Para a reação A ↔ 2B, partindo de “A” puro, o gráfico a seguir representa a variação das concentrações de “A” e “B” em função do tempo.
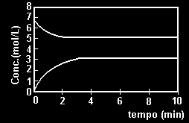
Para essa reação, a constante estequiométrica de equilíbrio, nessas condições, vale
a) 0,60
b) 0,83
c) 1,20
d) 1,67
e) 1,80
2) (Fuvest 99) – Algumas argilas do solo têm a capacidade de trocar cátions de sua estrutura por cátions de soluções aquosas do solo. A troca iônica pode ser representada pelo equilíbrio:
R–Na+(s) + NH4+(aq) ↔ R–NH4+(s) + Na+ (aq),
onde R representa parte de uma argila.
Se o solo for regado com uma solução aquosa de uma adubo contendo NH4NO3, o que ocorre com o equilíbrio anterior?
a) Desloca-se para o lado Na+(aq).
b) Desloca-se para o lado do NH4+(aq).
c) O valor de sua constante aumenta.
d) O valor de sua constante diminui.
e) Permanece inalterado.
3) (UFRGS/11) – A constante de equilíbrio da reação de conversão abaixo tem o valor de 0,5.
Glicose 6-Fosfato ↔ Frutose 6-Fosfato
Se essa reação parte de Glicose 6-Fosfato pura, o grau de conversão deste reagente em produto, quando a reação atinge o equilíbrio, é de aproximadamente
a) 10%
b) 25%
c) 33%
d) 50%
e) 66%
4) ENEM 2010 – Às vezes, ao abrir um refrigerante, percebe-se que uma parte do produto vaza rapidamente pela extremidade do recipiente. A explicação para esse fato está relacionada à perturbação do equilíbrio químico existente entre alguns dos ingredientes do produto de acordo com a equação:
A alteração do equilíbrio anterior, relacionada ao vazamento do refrigerante nas condições descritas, tem como consequência a:
a) Liberação de CO2 para o ambiente.
b) Elevação da temperatura do recipiente.
c) Elevação da pressão interna do recipiente.
d) Elevação da concentração de CO2 no líquido.
e) Formação de uma quantidade significativa de H2O.
5) (Fatec) – Nas condições ambientes, é exemplo de sistema em estado de equilíbrio uma:
a) xícara de café bem quente;
b) garrafa de água mineral gasosa fechada;
c) chama uniforme de bico de Bunsen;
d) porção de água fervendo em temperatura constante;
e) tigela contendo feijão cozido.
6) (Ufc) – Uma das reações que podem ocorrer em uma atmosfera poluída é representada pelo equilíbrio químico a seguir: 2NO(g) + O2(g) ↔ 2NO2(g); ∆H > 0.
Considerando tratar-se de uma reação simples e elementar, analise as afirmativas a seguir e marque a alternativa correta.
a) A ordem total da reação é 2.
b) Aumentando-se a pressão do sistema, não se altera a posição do equilíbrio.
c) Aumentando-se a temperatura do sistema, o equilíbrio desloca-se para a esquerda.
d) A reação é de terceira ordem, com relação ao NO, e de primeira ordem, com relação ao O2.
e) A reação é de segunda ordem, com relação ao NO, e de primeira ordem, com relação ao O2.
e) A reação é de segunda ordem, com relação ao NO, e de primeira ordem, com relação ao O2.
7) (Ufac) – Uma reação atinge o equilíbrio químico:
I. Quando não há mais reagentes, somente produtos.
II. Quando as concentrações dos reagentes são iguais às concentrações dos produtos.
III. Quando a velocidade da reação direta é igual à velocidade da reação inversa.
IV. Quando as concentrações de reagentes e produtos tornam-se constantes.
V. Quando não existe mais reação química.
As afirmações corretas são:
a) I e II
b) II e III
c) III e IV
d) IV e V
e) III e V
8) (FUVEST) – No sistema em equilíbrio:
2NO(g) + O2(g) —> 2NO2(g) ΔH = -27
a quantidade de NO2 aumenta com a:
a) diminuição de um catalisador.
b) diminuição da concentração de O2.
c) diminuição da temperatura.
d) diminuição da pressão.
e) introdução de um gás inerte.
9) (UFPB) – No mundo atual, são produzidas milhões de toneladas de compostos nitrogenados, entre os quais os fertilizantes são os mais importantes pelo papel que desempenham na produção de alimentos. Esses adubos agrícolas nitrogenados são fabricados a partir da amônia, que é produzida industrialmente através da síntese de Haber-Bosch, descrita pela seguinte equação:
N2(g) + 3 H2(g) ⇄ NH3(g) ∆H = -113 kJ/mol
Considerando a equação e a condição de equilíbrio do sistema, é correto afirmar que o rendimento da produção de amônia:
a) diminui com a remoção de NH3.
b) aumenta com a elevação da temperatura.
c) aumenta com o aumento da concentração de H2.
d) permanece inalterado com a diminuição da concentração de N2.
e) permanece inalterado com a redução do volume do reator.
10) (UFCSPA) – Acima de 330ºC o cloreto de amônio produz amônia e ácido clorídrico através de uma reação de decomposição, como mostra a equação abaixo:
NH4Cl(s) ⇄ NH3(g) + HCl(g)
Considerando que o sistema acima atingiu o equilíbrio, assinale a alternativa incorreta.
a) Ao se diminuir o volume do sistema acima haverá deslocamento de equilíbrio para a formação de cloreto de amônio. 8
b) Inserindo-se amônia no sistema haverá deslocamento de equilíbrio para a formação de cloreto de amônio.
c) A expressão matemática para a constante de equilíbrio expressa em termos de pressão (Kp) é dada por: Kp = [NH3].[HCl]/[NH4Cl]
d) Considerando que a pressão da mistura gasosa seja de 2,0 atm num determinado volume e temperatura, o valor numérico de sua constante Kp será 1,0.
e) O equilíbrio químico acima é um equilíbrio dinâmico.
11) (Mackenzie) – Seja a reação:
2 NaHCO3(s) ⇄ Na2CO3(s) + H2O(g) + CO2(g)
Qual é a expressão de Kp?
12) Unicamp 2014 – A equação abaixo mostra o equilíbrio químico em meio aquoso de uma droga muito utilizada no tratamento de náuseas e vômitos e também como antialérgico. Essa droga, dependendo da finalidade, pode ser comercializada na sua forma protonada (A) ou na sua forma neutra (B).
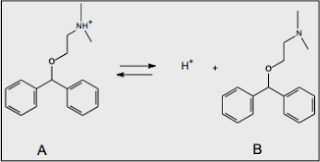
a) Sabendo-se que em meio aquoso a constante de equilíbrio para essa equação é igual a 1,2 x 10^-9 , qual espécie estaria em maior concentração no intestino (cujo pH é igual a 8): a protonada (A), a neutra (B) ou ambas estariam na mesma concentração? Justifique sua resposta com base em cálculos matemáticos.
b) Supondo que a droga seria absorvida de forma mais completa e com melhor efeito terapêutico se fosse mais solúvel em lipídios, qual forma seria preferível numa formulação, a protonada ou a neutra? Justifique sua resposta em termos de interações intermoleculares.
13) (UFPE) – Óxidos de nitrogênio, NOx , são substâncias de interesse ambiental, pois são responsáveis pela
destruição de ozônio na atmosfera, e, portanto, suas reações são amplamente estudadas. Num dado experimento, em um recipiente fechado, a concentração de NO2 em função do tempo apresentou o seguinte comportamento:
destruição de ozônio na atmosfera, e, portanto, suas reações são amplamente estudadas. Num dado experimento, em um recipiente fechado, a concentração de NO2 em função do tempo apresentou o seguinte comportamento:
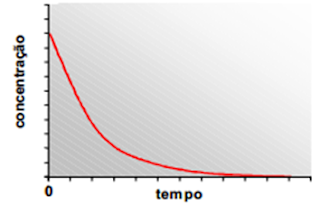
O papel de NO2 nesse sistema reacional é:
a) reagente.
b) intermediário.
c) produto.
d) catalisador.
e) inerte.
14) (CEFET–PR) – Com relação ao equilíbrio químico, afirma-se:
I. O equilíbrio químico só pode ser atingido em sistema fechado (onde não há troca de matéria com o meio ambiente).
II. Num equilíbrio químico, as propriedades macroscópicas do sistema (concentração, densidade, massa e cor) permanecem constantes.
III. Num equilíbrio químico, as propriedades microscópicas do sistema (colisões entre as moléculas, formação de complexos ativados e transformações de umas substâncias em outras) permanecem em evolução, pois o equilíbrio é dinâmico.
É (são) correta(s) a(s) afirmação(ões):
a) Somente I e II.
b) Somente I e III.
c) Somente II e III.
d) Somente I.
e) I, II e III.
15) (PUC-RJ) – Reações químicas dependem de energia e colisões eficazes que ocorrem entre as moléculas dos reagentes. Em sistema fechado, é de se esperar que o mesmo ocorra entre as moléculas dos produtos em menor ou maior grau até que se atinja o chamado “equilíbrio químico”.
O valor da constante de equilíbrio em função das concentrações das espécies no equilíbrio, em quantidade de matéria, é um dado importante para se avaliar a extensão (rendimento) da reação quando as concentrações não se alteram mais.
Considere a tabela com as quantidades de reagentes e produtos no início e no equilíbrio, na temperatura de 100°C, para a seguinte reação:
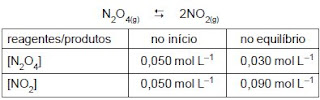
A constante de equilíbrio tem o seguinte valor:
a) 0,13
b) 0,27
c) 0,50
d) 1,8
e) 3,0
16) PUC/PR 2015 – O gás contido no refrigerante que consumimos é o gás carbônico (dióxido de carbono – CO2). Geralmente, o refrigerante é formado por uma solução aquosa de um tipo de xarope e esse gás. Antes de misturar o gás no xarope, os fabricantes misturam a água e o gás num aparelho chamado carbonizador, gerando o ácido carbônico. Nesse tipo de bebida existe, então, o seguinte equilíbrio químico:

Sobre o equilíbrio químico apresentado são feitas as seguintes afirmações:
I. A elevada acidez presente no estômago devido à presença do ácido clorídrico faz com que o equilíbrio seja deslocado para a esquerda, favorecendo a liberação do gás carbônico.
II. Um aumento na pressão total do sistema provocará uma diminuição do pH do refrigerante. III. Um aumento na temperatura aumenta a solubilidade do gás carbônico, deslocando o equilíbrio para a direita.
IV. A adição de um catalisador apropriado aumentará a acidez do refrigerante.
São VERDADEIRAS:
A) somente as afirmações II e III.
B) somente as afirmações I e III.
C) somente as afirmações II e IV.
D) somente as afirmações III e IV.
E) somente as afirmações I e II.
17) (FFFCMPA) – Em um reator isotérmico de volume constante, à temperatura de 700 K, são colocados 9 mols de BrCl e estabelece-se o equilíbrio 2 BrCl(g) –> Br2(g) + Cl2(g). Sabendo-se que a constante de equilíbrio, Kc, dessa reação é igual a 16, o número de mols de Br2 presentes no equilíbrio será igual a
a) 2,0
b) 4,0
c) 5,0
d) 7,2
e) 8,0
18) (ENEM 2009) – Sabões são sais de ácidos carboxílicos de cadeia longa utilizados com a finalidade de facilitar, durante processos de lavagem, a remoção de substâncias de baixa solubilidade em água, por exemplo, óleos e gorduras. A figura a seguir representa a estrutura de uma molécula de sabão.
Em solução, os ânions do sabão podem hidrolisar a água e, desse modo, formar o ácido carboxílico correspondente. Por exemplo, para o estearato de sódio, é estabelecido o seguinte equilíbrio:
Uma vez que o ácido carboxílico formado é pouco solúvel em água e menos eficiente na remoção de gorduras, o pH do meio deve ser controlado de maneira a evitar que o equilíbrio acima seja deslocado para a direita.
Com base nas informações do texto, é correto concluir que os sabões atuam de maneira:
A) mais eficiente em pH básico.
B) mais eficiente em pH ácido.
C) mais eficiente em pH neutro.
D) eficiente em qualquer faixa de pH.
E) mais eficiente em pH ácido ou neutro.
13
Visitas totales
12
Visitantes únicos
